Die Kammerquantifizierung ist ein entscheidender Bestandteil der transthorakalen Echokardiographie (TTE) und umfasst das enddiastolische und endsystolische Volumen des linken Ventrikels (LV; EDV, ESV), das maximale endsystolische Volumen des linken Herzvorhofs (LA) sowie die LV-Ejektionsfraktion (LVEF). Tatsächlich empfehlen die kürzlich veröffentlichten Leitlinien 1 zur Kammerquantifizierung, dass zwei- oder dreidimensionale echokardiographische (2DE, 3DE) Messungen der LV- und LA-Volumina routinemäßig im Rahmen aller klinischen Studien durchgeführt werden sollten.
Heute ist Echtzeit-3DE ein wertvolles Tool zur Bewertung von LV- und linker Herzvorhof-Volumina sowie Ejektionsfraktion. Zahlreiche Studien belegen, dass 3DE genauer und reproduzierbarer ist als 2DE, da eine direkte Messung der Volumina möglich ist, ohne die Anforderung geometrischer Annahmen über die Kavitätenform und Einschränkungen bei verkürzten Ansichten.
Trotz der bekannten Vorteile von 3DE wird diese Modalität aus verschiedenen Gründen in der klinischen Praxis nicht routinemäßig eingesetzt, darunter (1) die Anforderung an 3DE-spezifische Fachkenntnis und (2) die zusätzliche Zeit für die 3DE-Bildgebung. Für die routinemäßige Durchführung von 3DE in der klinischen Praxis ist die Implementierung einer automatisierten Quantifizierung erforderlich, um Unterbrechungen oder Verzögerungen im Arbeitsablauf zu vermeiden.
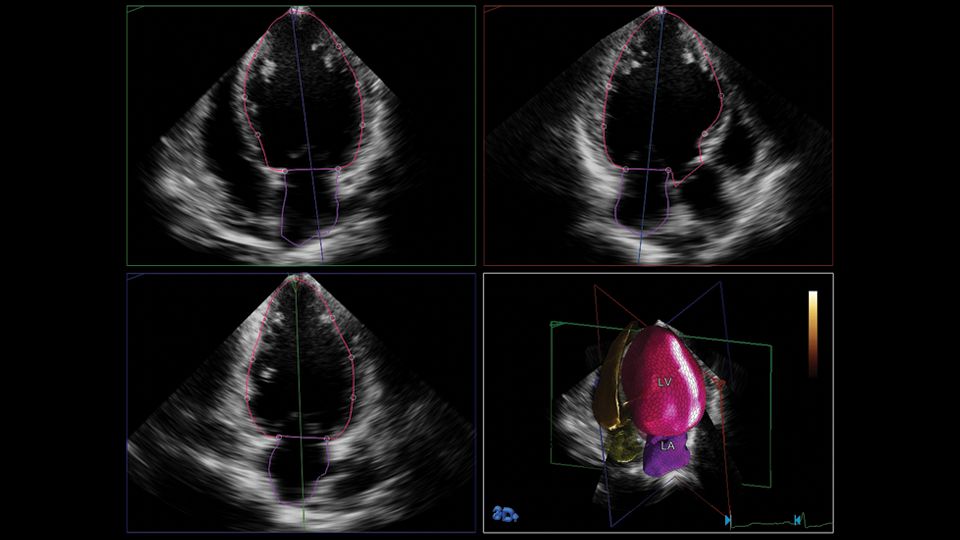
Philips hat vor Kurzem HeartModel entwickelt – eine vollautomatisierte 3D-TTE-Applikation, die simultan die Endokardoberflächen von linker Herzvorhof und LV über den gesamten Herzzyklus erkennt und dabei einen adaptiven Analyse-Algorithmus verwendet, der aus einer wissensbasierten Identifikation der initialen globalen Form und Orientierung mit anschließender patientenspezifischer Anpassung besteht (Abbildung 1). Der Prozess beginnt damit, dass das Programm mittels Bewegungsanalyse nahe der Spitze der elektrokardiographischen R-Zacke den LV-enddiastolischen (ED) Bildbereich schätzt. Mit diesem Bildbereich werden die allgemeine Form und Ausrichtung identifiziert, und anschließend wird der LV-endsystolische (ES) Bildbereich mittels Bewegungsanalyse geschätzt, um die kleinste LV-Kavität zu bestimmen. Sobald die LV-ED- und ES-Frames geschätzt wurden, werden vorläufige ES- und ED-Modelle des LV und des linken Herzvorhofs unter Verwendung der automatisch detektierten endokardialen Oberfläche in Verbindung mit Informationen aus einer 3D-TTE-Datenbank des linken Herzvorhofs und des LV erstellt. Diese Datenbank enthält eine Vielzahl von Formen des linken Herzvorhofs (LA) und der linken Herzkammer (LV) in enddiastolischer (ED) und endsystolischer (ES) Phase, die aus etwa 1.000 3D-TTE-Datensätzen unterschiedlicher Bildqualität von Patient*innen mit einer großen Bandbreite an Kammergröße und Funktion gewonnen wurden. Das Programm vergleicht Merkmale des analysierten LV-Volumens mit ausgewählten Formen in der Datenbank. Diese ausgewählte Form wird anschließend mittels einer Reihe von schrittweisen Anpassungen lokal an das untersuchte LV-Volumen angepasst. Die ED- und ES-Phasen werden dann schließlich erkannt, indem die LV-Volumina im Bereich von Enddiastole und Endsystole ausgewertet und jeweils die Phase mit dem max. bzw. min. Volumen ausgewählt wird. Der Algorithmus wurde so konzipiert, dass er sich an verschiedene Bildgebungsbedingungen anpasst, darunter Bildausfälle (Dropout), Schall-Clutter-Artefakte, ventrikuläre Form und die Ausrichtung des Herzens relativ zum Schallkopf. Ähnlich wie bei manuellen Messungen ist jedoch eine min. Anzahl von sichtbaren Endokardkontur-Segmenten (~14–15 von 17 LV-Segmenten) erforderlich, damit eine genaue Schätzung des Kammervolumens abgeleitet werden kann. Schließlich zeigt der Algorithmus, wenn er mit demselben Datensatz ausgeführt wird, eine deterministische Konvergenzantwort, wodurch keine Variabilität entsteht. Nachdem das endgültige Modell angepasst wurde, werden die LA- und LV-Konturen auf 2D-Schnittebenen angezeigt, die aus den 3DE-Datensätzen abgeleitet sind und die ES- und ED-Ansichten der 4-, 3- und 2-Kammer-Blick zeigen (Abbildung 2). Falls Anwender*innen mit den LA- und LV-Konturen nicht zufrieden sind, können diese manuell bearbeitet werden.

Abbildung 1

Abbildung 2
Diese neue vollautomatisierte Applikation wurde kürzlich validiert und erwies sich im Vergleich zu manuellen 3D-Messwerten mit QLAB (3D-Quantifizierung des Herzens (3DQ))2 bei einer Gruppe von über 150 Patient*innen an der University of Chicago als hinreichend genau. Diese vielversprechende Software bietet das Potenzial, 3DE-basierte LV- und linker Herzvorhof-Messungen in die routinemäßigen klinischen Arbeitsabläufe weltweit zu integrieren.
In dieser Studie zielten wir darauf ab, das Zeiteinsparungspotenzial dieser neuartigen Applikation im Vergleich zu klassischen 2DE- und 3DE-Methoden zur Messung des LV- und linken Herzvorhof-Volumens zu evaluieren.
Bei 30 aufeinanderfolgenden Patient*innen wurde die 2DE- und 3DE-Bildgebung unter Verwendung eines EPIQ-Systems mit einem X5-1 Schallkopf (Philips, Andover, MA) durchgeführt. Es wurde die Zeit aufgezeichnet, die für die Erfassung der 2DE LV-apikalen 4-Kammer- (A4C) und apikalen Zweikammeransicht (A2C) Ansichten, der linker Herzvorhof (LA)-A4C- und apikalen Zweikammeransicht (A2C) Ansichten sowie eines 3DE-Komplettvolumendatensatzes von LV und linker Herzvorhof (LA) benötigt wurde. Zusätzlich wurde aufgezeichnet, wie viel Zeit für die Volumenmessung von LV (enddiastolisch und endsystolisch) und linker Herzvorhof (Endsystole) mithilfe der Biplan-Scheibchenmethode aus den 2DE-Bildern benötigt wurde. Abschließend wurde die für die Analyse der 3DE-Datensätze zur Bestimmung der LV- und LA-Volumina mit QLAB und der neuen HeartModel-Applikation benötigte Zeit aufgezeichnet. Die HeartModel-Analyse wurde sowohl auf einem Standard-PC als auch im EPIQ-Bildgebungssystem mit und ohne globale und regionale Anpassungen durchgeführt.

Tabelle 1
Tabelle 1 zeigt die Daten zu den Zeiten, die für die Erfassung und Analyse benötigt wurden. Insgesamt benötigte die 3DE-Bilderfassung weniger Zeit als die für die Volumenmessungen erforderlichen 2DE-Ansichten. Zudem erfolgte die Auswertung der 3DE-Bilder deutlich schneller als die der 2DE-Bilder, und die Analysezeit verkürzte sich durch die automatisierte HeartModel-Software weiter (Abbildung 3). Hervorzuheben ist, dass die Gesamtzeitersparnis für Erfassung und Analyse kombiniert in der vollautomatischen Betriebsart 82 % und selbst bei manueller Nachbearbeitung 63 % betrug.
Um die Zeitersparnis, die HeartModel pro Tag in einem vielbeschäftigten Echokardiographie-Labor mit 50 täglichen TTE-Untersuchungen bieten kann, vollständig zu berechnen, multiplizierten wir die kombinierte Erfassungs- und Analysezeit mit 50 (siehe Abbildung 4). Dieses repräsentative Beispiel zeigt, dass die Erfassung und Auswertung der LV- und linker Herzvorhof-Volumina mittels 2DE fast 3 h pro Tag beansprucht, während mit HeartModel und geringfügiger Nachbearbeitung nur 66 Minute und in der vollautomatischen Betriebsart etwas mehr als eine halbe h erforderlich sind, wodurch ein typisches Echokardiographie-Labor täglich 2,5 h spart.

Abbildung 3

Abbildung 4
Ein repräsentatives Beispiel zeigt, dass die Erfassung und Auswertung der LV- und linker Herzvorhof-Volumina mit 2DE fast drei h pro Tag in Anspruch nimmt, während mit HeartModelA.I. und geringfügiger Nachbearbeitung nur 66 Minuten und in der vollautomatischen Betriebsart etwas mehr als eine halbe h erforderlich wären.
Untersuchungen mehrerer Forscher*innen haben ergeben, dass die 3DE genauer und reproduzierbarer ist als die 2DE. Um den routinemäßigen Einsatz der 3DE-Technologie in klinischen Laboren zu ermöglichen, besteht die Anforderung, automatisierte Verfahren zu implementieren, die den zeitintensiven Arbeitsfluss, den 3DE derzeit mit sich bringt, überwinden. Die neue vollständig automatisierte HeartModel-Applikation wurde kürzlich validiert und hat sich im Vergleich zur manuellen 3DE-(QLAB)-Analyse (3D-Quantifizierung des Herzens (3DQ)) als genau und reproduzierbar erwiesen. In unserer Studie zeigte sich, dass dieses neue vollautomatische Tool deutlich schneller ist als sowohl die 2DE- als auch die manuelle 3DE-(QLAB)-Analyse und somit dazu beitragen kann, die zeitintensive 3DE-Analyse, die derzeit ihre Nutzung einschränkt, zu überwinden und ihre Integration in den klinischen Arbeitsablauf zu erleichtern.

Automatische transthorakale 3D-Echoquantifizierung der Linksherz-Kammern